近日,药学科学学院沈玉先教授团队在国际知名期刊《细胞报道(Cell Reports)》(中科院一区TOP)发表题为《HRD1通过抑制SNAP29液-液相分离负调控自噬溶酶体形成(HRD1 negatively regulates autolysosome formation by inhibiting liquid-liquid phase separation of SNAP29)》的研究论文。基础医学博士后科研流动站瞿文艳博士为第一作者,沈玉先教授为本文通讯作者。我校为论文的第一完成单位和通讯作者单位。
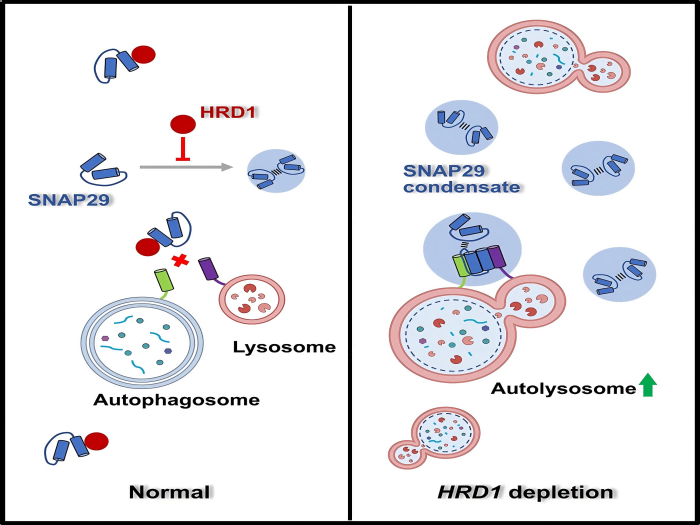
自噬是真核细胞中高度保守的降解过程,通过自噬体与溶酶体融合形成自噬溶酶体,实现对胞质内容物的清除。SNARE蛋白介导的膜融合是自噬体与溶酶体结合的关键步骤,然而其精细调控机制尚未完全阐明。近年来,液-液相分离(LLPS)被发现广泛参与细胞多种生理过程的调控,但其是否参与自噬过程中SNARE复合体的组装及功能调节仍不清楚。为此,该研究团队系统探究了E3泛素连接酶HRD1在自噬调控中的作用,首次揭示了HRD1通过调控SNAP29的液-液相分离过程,影响SNARE复合体的组装效率,进而调控自噬体-溶酶体融合与自噬进程。研究发现,HRD1缺失能够显著促进自噬流及自噬溶酶体形成,该过程依赖于SNARE蛋白SNAP29。进一步研究表明,SNAP29在体内外均可形成高度动态的液相凝聚体,且该凝聚体的形成是SNARE复合体高效组装的重要基础。机制上,HRD1通过其胞质结构域直接与SNAP29互作,抑制其发生相分离凝聚。而当HRD1缺失时,SNAP29凝聚体形成增强,进而促进SNARE复合体组装与自噬体-溶酶体融合。
本研究首次建立了HRD1–SNAP29液液相分离–SNARE组装–自噬溶酶体形成的调控轴线,揭示了蛋白质相分离在自噬膜融合过程中的关键作用,为理解自噬过程的时空动态调控提供了新视角,也为相关疾病的机制研究与潜在靶点开发提供了新思路。
该研究得到了国家自然科学基金区域创新联合基金重点项目、国家自然科学基金青年项目、国家自然科学基金面上项目以及安徽省教育厅科研项目的资助。(药学科学学院)
原文链接:https://doi.org/10.1016/j.celrep.2025.116914


