1月15日,华体会平台校长、中国科学技术大学讲席教授翁建平、郑雪瑛研究员团队在双一区期刊《代谢(Metabolism)》 (IF=11.9)发表了题为《整合功能基因组学与精细定位鉴定多变量肥胖 GWAS 的调控机制及其代谢影响(Integrative Functional Genomics and Fine-Mapping Identify Regulatory Mechanisms of Multivariate Obesity GWAS and Its Cardiometabolic Implications)》的研究论文,通过构建多性状、多组学整合分析框架,系统揭示了肥胖背后的“神经-脂肪调控轴”遗传机制,为精准代谢干预提供了全新的遗传学依据。该研究在中国科学院战略性先导科技专项(B 类)、国家重点研发计划、国家自然科学基金联合基金重大项目、安徽省临床医学研究与转化专项及安徽省教育厅高校科研项目等多项基金资助下完成。华体会平台博士研究生王穗健、刘四化为论文共同第一作者。
肥胖并非单一性状,而是一种由中枢神经系统与脂肪组织共同调控的系统性疾病,其遗传基础高度复杂,长期以来难以被传统单一性状全基因组关联研究(GWAS)全面解析。
现有研究多以体重指数(BMI)作为肥胖表型,但无法区分内脏脂肪、肝脏脂肪等对代谢和心血管风险具有决定性影响的脂肪分布类型,限制了对肥胖遗传机制及精准干预靶点的发现。
该研究整合了体重指数(BMI)、腰围、体脂率、内脏脂肪和肝脏脂肪五项关键肥胖相关性状,利用基因组结构方程模型(Genomic SEM)构建潜在多变量肥胖表型(mvObesity),并在超过 300 万有效样本量的基础上开展多变量全基因组关联分析。
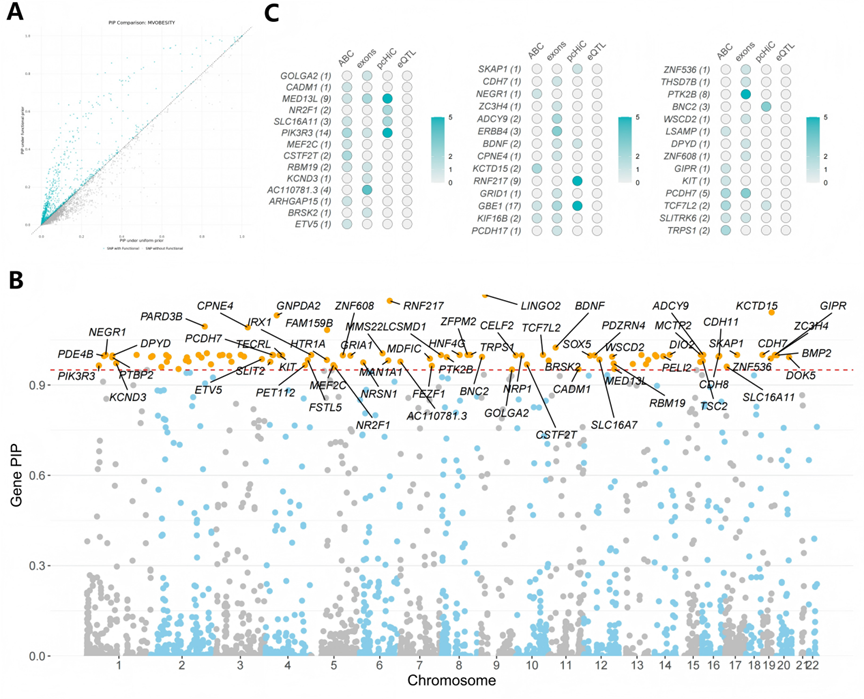
研究结果显示,多变量分析共鉴定出 548 个肥胖相关遗传位点,其中 45 个为传统单性状 GWAS 未能发现的新信号,显著提升了遗传发现能力。进一步结合脂肪组织染色质可及性、增强子-启动子互作、eQTL 数据以及转录组和蛋白组遗传预测分析(TWAS / PWAS),研究团队从非编码变异出发,系统解析了其潜在的调控靶基因。
通过精细定位与多组学证据整合,研究最终优先筛选出 150 个高置信度候选基因。功能富集分析显示,这些基因不仅参与脂质代谢和转录调控过程,更显著富集于神经信号传导、突触结构和神经发育相关通路,提示中枢神经系统在肥胖发生中的关键调控作用。MAGMA 分析进一步揭示,这些基因在小脑、海马、下丘脑、伏隔核等脑区呈现显著富集,指向跨组织的神经-代谢调控网络。
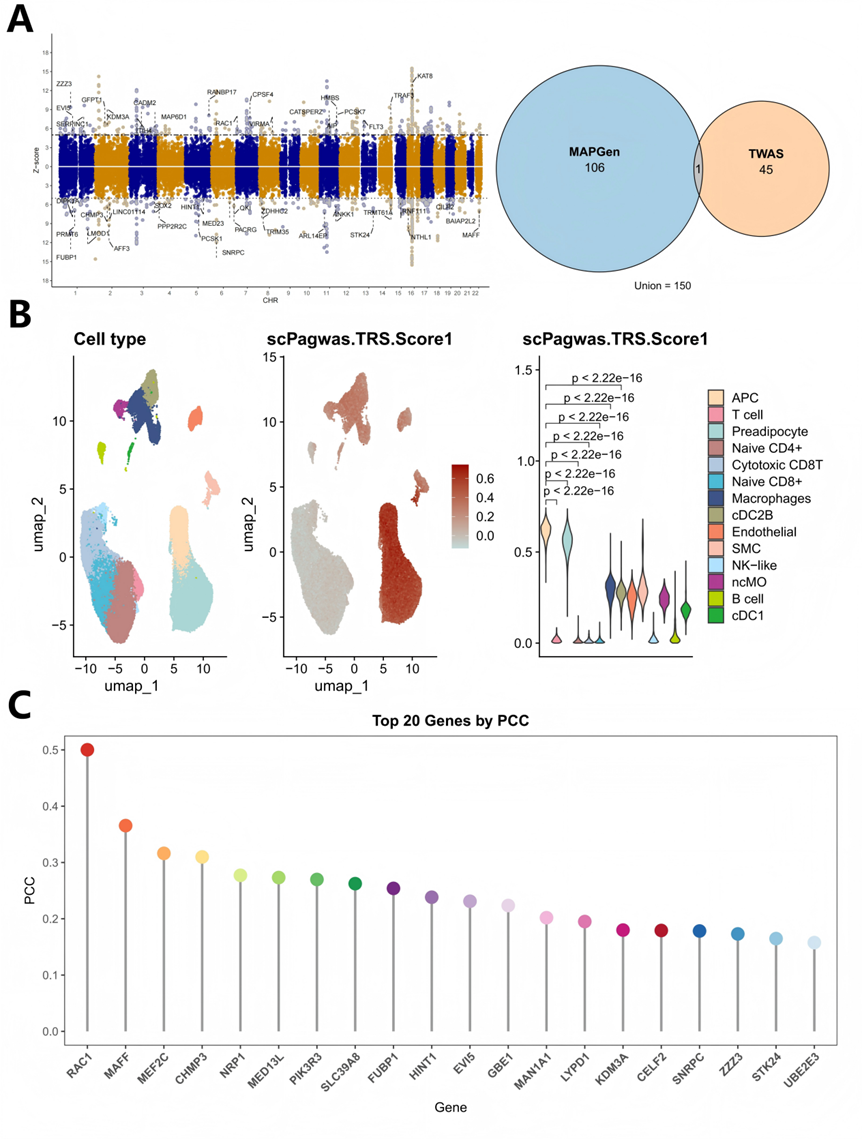
在单细胞层面,研究发现肥胖相关遗传风险主要富集于脂肪前体细胞、前脂肪细胞和平滑肌细胞,并在脑组织中显著富集于内皮细胞、免疫细胞和胶质细胞。多组织 TWAS 与单细胞转录组分析一致支持神经系统与脂肪组织之间存在协同的转录调控模式。
值得关注的是,研究还在多个独立人群的血浆蛋白组参考队列中验证了部分关键基因在蛋白水平上的遗传效应,其中 CADM2、PCSK1、SLIT2 等基因在多个队列中表现出一致关联,进一步增强了结果的稳健性与转化潜力。
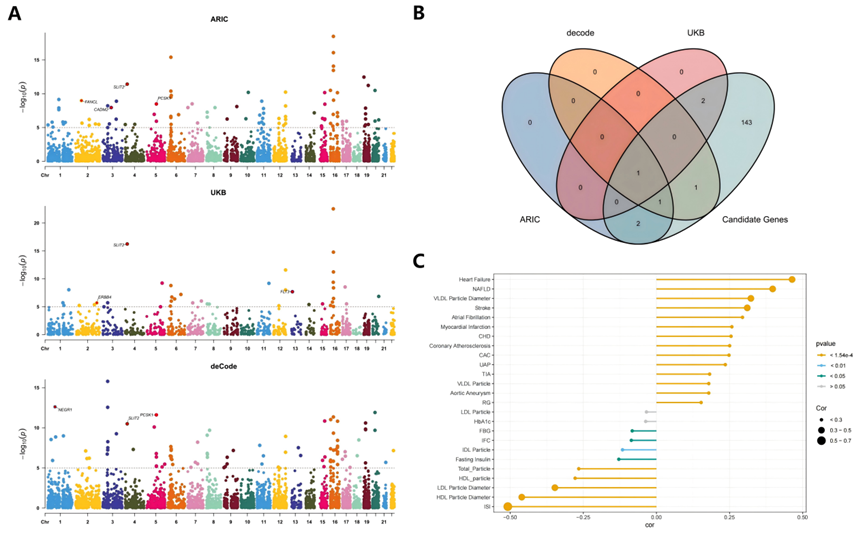
此外,全基因组及局部遗传相关分析显示,mvObesity 与心力衰竭、冠心病、房颤、非酒精性脂肪肝及多项脂蛋白代谢表型存在显著遗传重叠,提示肥胖相关遗传变异在心血管-代谢疾病中的广泛多效性作用。
通过整合精细定位、转录组、蛋白组、单细胞表达、遗传共定位等七个层面的独立证据,研究最终锁定了一批高度一致的核心调控基因,包括 MED13L、GBE1、CADM2、PIK3R3、ERBB4、PTK2B 和 TCF7L2 等。这些基因在脂肪与脑组织中呈现高度一致的遗传调控信号,构成潜在的“神经-脂肪调控枢纽”。
综上所述,该研究通过多变量 GWAS 与多组学整合分析,系统描绘了肥胖的跨组织遗传调控网络,首次从遗传学层面明确提出“神经-脂肪调控轴”在肥胖发生与心代谢并发症中的核心作用。
该研究不仅为理解肥胖的系统性本质提供了新的理论框架,也为未来基于遗传证据的精准代谢干预和靶点开发奠定了坚实基础。
原文链接:https://www.metabolismjournal.com/article/S0026-0495(26)00018-1/abstract


